公司新闻/正文
升级版CART细胞来啦,看肿瘤抗原还往哪里逃!
人阅读 发布时间:2019-08-16 14:58
CAR-T ,全称Chimeric Antigen Receptor T-Cell Immunotherapy,嵌合抗原受体T细胞免疫疗法。被认为是最有前景的肿瘤治疗方式之一。
近年来,研究人员对CAR-T的研究又更进了一步,他们通过一个由15个氨基酸组成linker将IL13突变蛋白和HER2单链抗体连接起来。与CD3 ζ、CD28胞内信号链形成一个『双价二代CAR分子』,称之为『串联CAR』或者『TanCAR』。
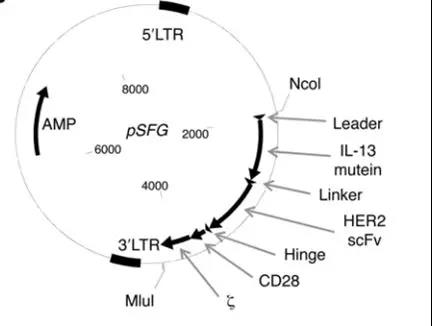
TanCAR-T同时识别HER2和IL13Rα2的效应『高于单个识别的累加效应,而且T细胞活性更持久,表现出优越的溶解自体恶性胶质瘤的能力,减缓肿瘤抗原逃逸现象。』
CAR T细胞治疗后GBM复发中存在抗原逃逸变体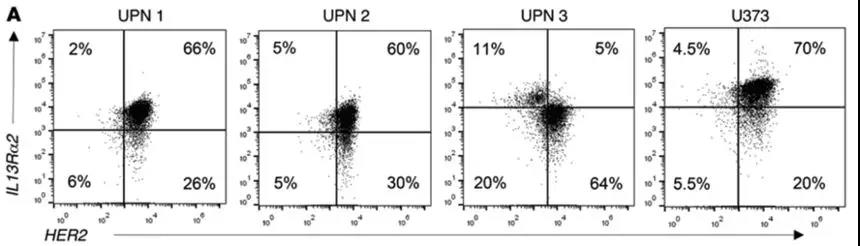
A:检测原发性GBM切除样品和U373的单细胞悬液HER2和IL13Rα2抗原的表达,并通过流式细胞术分析。
B: 过继转移后,使用共免疫荧光对HER2和IL13Rα2靶向HER2和IL13Rα2的CAR T细胞治疗后复发的U373异种移植物的分析。
注:【过继转移】即通过输注免疫细胞或免疫分子,将一个接触过抗原的个体(供体)所具有的免疫反应性被动地转移给未被免疫的个体。
构建和计算机查询HER2 /IL13Rα2二价CAR分子的结构功能
表1:将个体FRP5-scFv和IL-13突变蛋白结构域的能量分别对应HER2和IL13Rα2,TanCAR与HER2和IL13Rα2,以及集体对接

使用可溶性HER2和IL13Rα2来证实TanCAR外结构域与TAA的明显的非特异性以及双特异性结合
A:在离体培养物中表达稳定超过12周,检测UPN1,2和3在TanCAR T细胞处理后特异性地分泌IFN-γ和IL-2表达水平。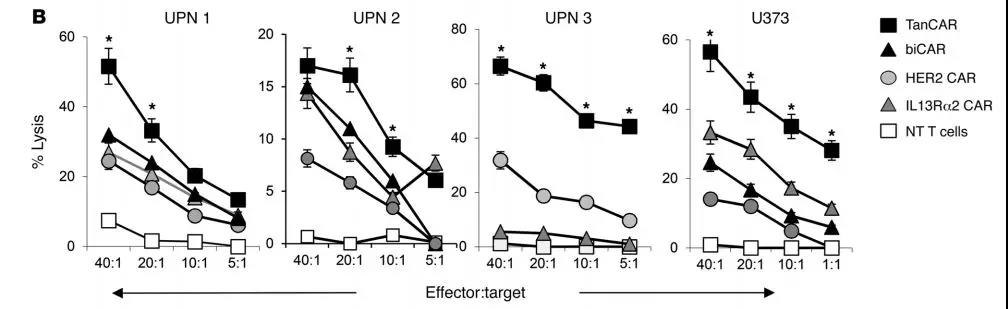
B:细胞溶解能力测定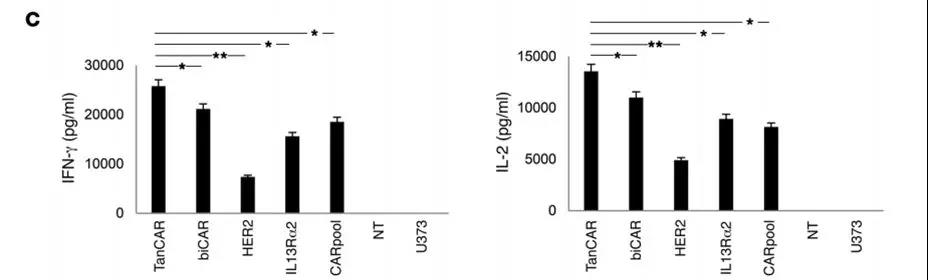
C:为了评估它们的相对细胞因子分泌能力,以1T细胞与4个肿瘤细胞的比例与TanCAR,biCAR,HER2,IL13rα2和CARpool T细胞共培养U373神经胶质瘤细胞。在24小时收集上清液,并使用ELISA分析IL-2和IFN-γ。
TanCAR T细胞以剂量依赖性方式与HER2或IL13Rα2接触被激活,并在同时遇到HER2和IL13Rα2时显示出超加性激活。
我们在涂有HER2.Fc,IL13Rα2.Fc(一种无关靶标)(GD2.scFv抗独特型)和非特异性T细胞受体兴奋剂的增加密度的平板上(OKT3)培养TanCAR T细胞。24小时分析上清液中IFN-γ和IL-2。
结果:当TanCAR T细胞在任何抗原密度下同时遇到任何一种TAA时,细胞因子产生显着增加(P <0.001),并且高于单次抗原接触时最大细胞因子浓度之和,表示遇到的超加性效应两种抗原分子。
TanCAR T细胞表现出增强的和持续的离体抗肿瘤活性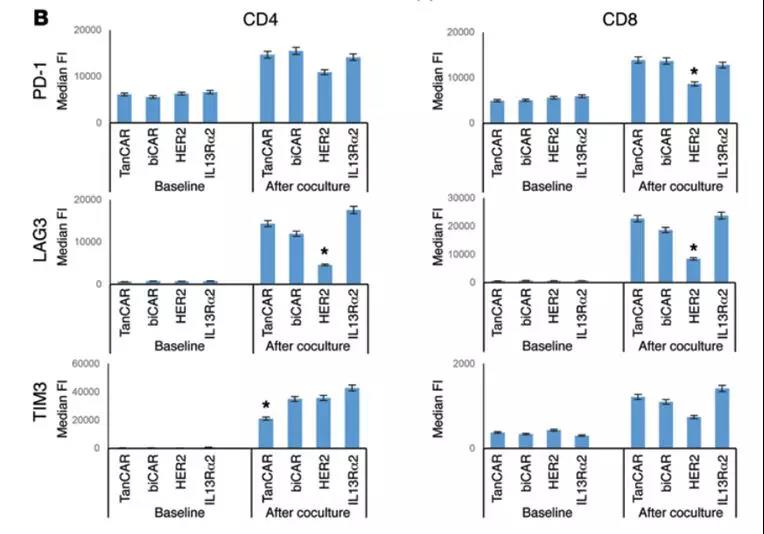
比较TanCAR,biCAR,CARpool和非特异性CAR T的抗肿瘤细胞活性的持续时间。基于电阻抗的肿瘤细胞培养系统(xCELLigence)。以1T细胞接种10个的U373细胞的比例,基于阻抗的细胞指数公式来量化肿瘤细胞的密度(图A)。在150小时的时间推移中评估U373神经胶质瘤细胞的实时杀伤。
B:以1T细胞与10个肿瘤细胞的比例接种1周后,评估CD4和CD8耗竭标志物PD-1,LAG3和TIM3的表达。
TanCARs在增强的二价免疫突触中异二聚化HER2和IL13Rα2。

研究TanCAR细胞是否是二价的,确定了它们的靶抗原在CAR T细胞-GBM接触点的定位。
将TanCAR,IL13Rα2CAR,HER2 CAR和NT T细胞与U373-GBM细胞一起温育,然后对HER2和IL13Rα2染色,可视化IS(免疫突触)(图B)
C:IS积累的定量揭示了,与非特异性T细胞相比,TanCAR IS中HER2和IL13Rα2的集体聚集增加。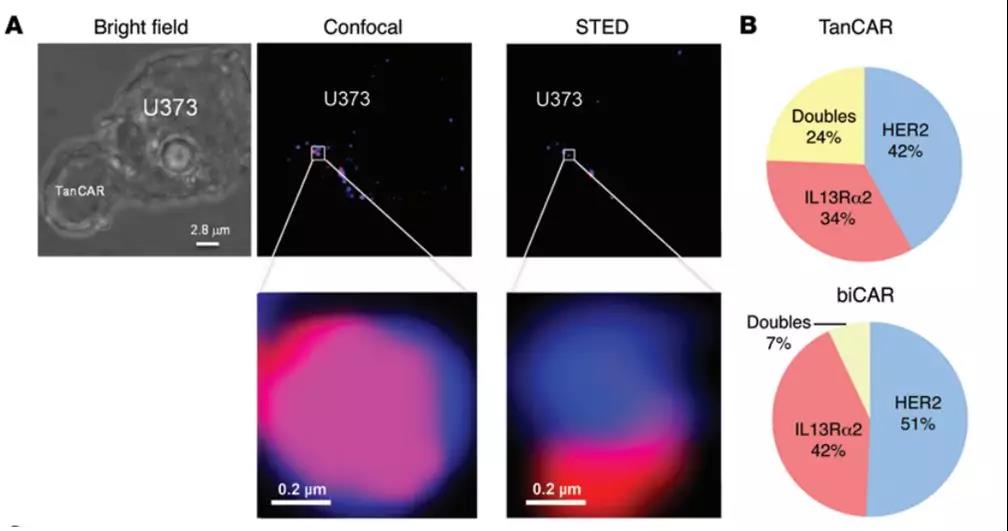
A:使用受激发射损耗(STED)超分辨率显微镜,利用连续波显微镜,我们成像TanCAR T细胞/ U373 ISs。
B:能够在TanCAR / U373 IS上以比biCAR / U373 IS更高的频率观察HER2和IL13Rα2配体异二聚体。
A 、B:HER2和IL13Rα2像素强度的线剖面显示足够高的分辨率,表明聚集体足以支持HER2和IL13Rα2与TanCAR外结构域的共同对接。
C:探测IS处的HER2-IL13Rα2异二聚体。在小于40nm的接近度内检测蛋白质 - 蛋白质相互作用。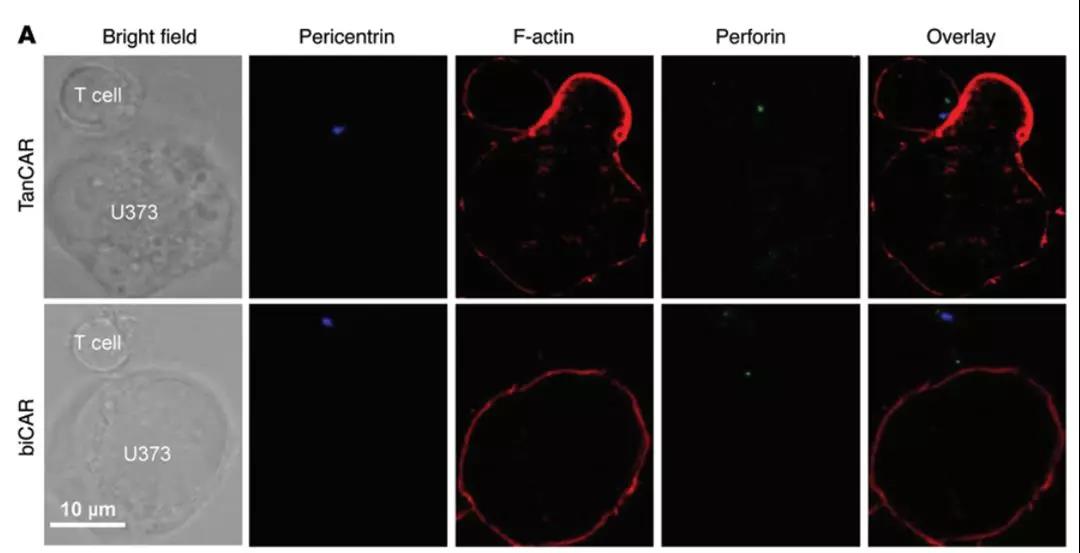
A:测量了IS处的F-肌动蛋白积累和微管组织中心的极化(MTOC),2种处理细胞的溶解参数,以评估TanCAR二价是否与功能优势相关。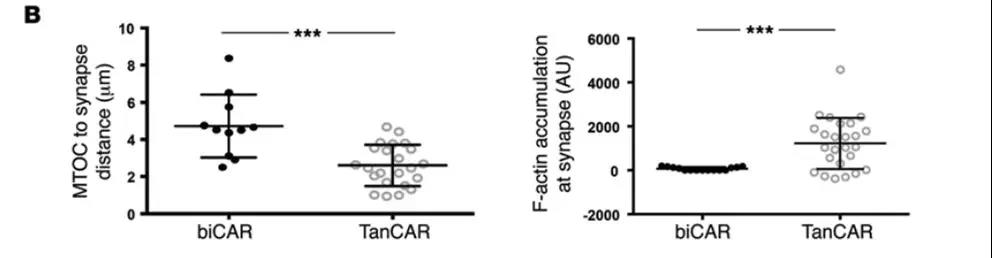
B:与biCAR T细胞相比,TanCAR T细胞显示出明显增加的ISOC MTOC极化,表明MTOC与IS的距离减少,以及IS处的F-肌动蛋白积累显着增加,从而表明具有优异的细胞溶解潜力。
总的来说,结果表明TanCART细胞在IS处共同募集并共同结合HER2和IL13Rα2,并且TanCAR介导的ISs具有显着更好的溶解潜力。通过双TAA IS的更高密度聚类,证明了将靶TAA募集到T细胞-GBM界面的能力,导致更强的T细胞活化。
TanCAR T细胞改善原位GBM的消除并减轻抗原逃逸。
A:GBM异种移植物用T细胞注射时,的每30个肿瘤细胞用约1T细胞处理。定量生物发光成像在预定时间点完成监测肿瘤生长。
B:肿瘤通过立体定位建立注射2.5×105表达eGFP-Firefly荧光素酶的U373细胞到SCID小鼠右侧额叶皮层。在肿瘤细胞注射后第8天,肿瘤内注射1×106处理小鼠TanCAR T细胞(n = 10),HER2 CAR T细胞(n = 10),IL13Rα2CAT T细胞(n = 10)或NT T细胞(n = 5)。预计的T细胞/ GBM细胞比率为1:30。未经治疗的老鼠(n = 5)用作对照。

B:无疾病进展生存期(Progression-free survival, PFS):PFS更侧重反映肿瘤治疗的中短期疗效。
C: 中位总生存期 (overall survival, OS):OS更侧重反映肿瘤治疗的整体结果。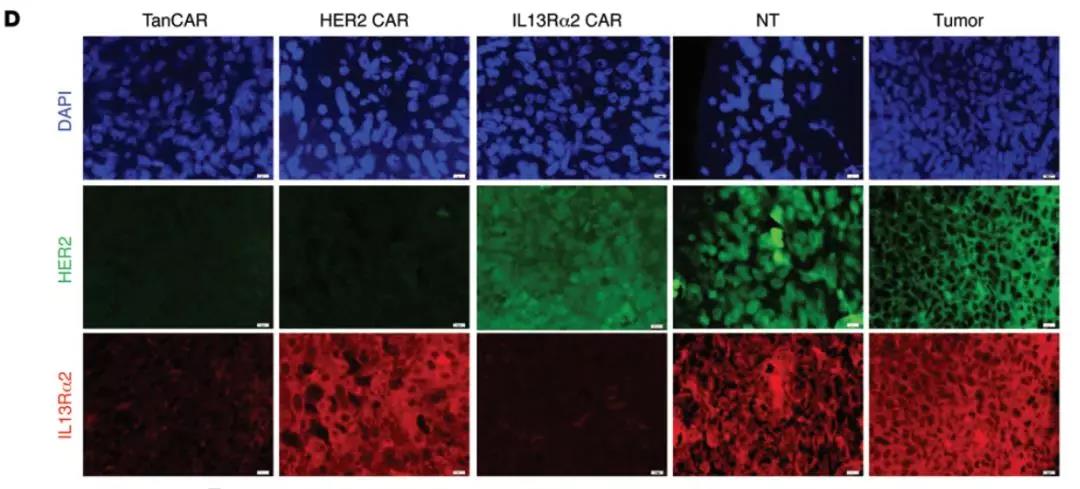
D:对HER2和IL13Rα2是昏暗染色。
E:TanCAR T细胞转移后的肿瘤复发通过生物发光成像显着减小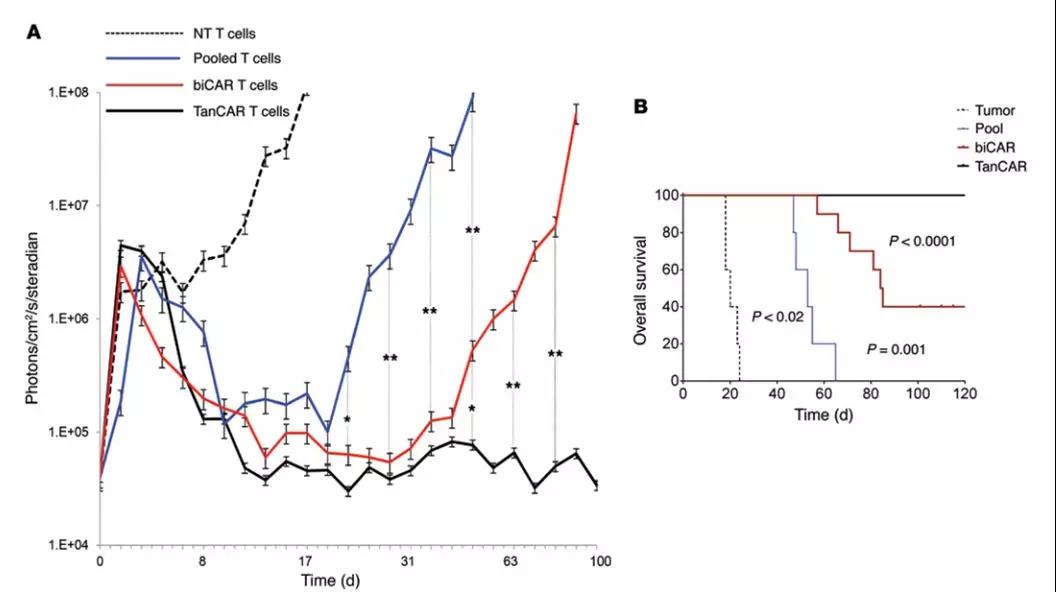
为了评估TanCAR T细胞与这些双特异性抗体的抗肿瘤功效,进行了第二次原位体内实验,其中在T细胞注射时每3个肿瘤细胞用约1T细胞处理已建立的原位GBM异种移植物。中位OS是主要结果。
结果:Pool:5只中0只存活(0%)
biCAR:10只中3只存活(30%)
TanCAR:13只全部存活(100%)
☞ 总 结 ✍
✔ TanCAR T细胞可清除胶质母细胞瘤模式小鼠体内的大多数癌细胞
✔ 阻止肿瘤抗原逃逸
✔ 基于靶向特异性表面分子,可以更好地控制肿瘤和改善小鼠存活的周期